不过,仿制产品不能在中国地区销售。

据辉瑞2月8日公布的2021年业绩报告数据显示,辉瑞在2021年实现营收813亿美,同比大涨92%。其中,口服抗病毒药物Paxlovid在2021年12月22日获得FDA的EUA批准后,已拿下美国政府2000万疗程订单,预计年底将实现1.2亿疗程产能。
对辉瑞来说,在新冠口服药上的竞争对手就是默沙东。根据默沙东披露的财报信息,2021年新冠口服药molnupiravir也贡献了9.52亿美的收入,预测在2022年molnupiravir的销售额将达到50亿~60亿美,2022年全球销售额将在561亿~576亿美之间。
另据默沙东公告,截至2021年底已生产1000万疗程Molnupiravir,预计2022年将生产至少2000万疗程Molnupiravir。
天风证券分析指出,从美国政府新冠药物采购数据可以看出,自新冠口服药上市后,美国政府采购抗体药物数量趋势下降,新冠口服药物采购趋势明显上涨。据各国政府报道,针对辉瑞Paxlovid,美国、英国、日本已分别累计采购2000万、275万、200万疗程;针对默沙东molnupiravir,美国、英国、日本已分别累计采购950万、230万和160万疗程。
在MPP协议之下,以Paxlovid和molnupiravir为代表的新冠小分子口服药成为下一个风口。不过,从现有的消息来看,MPP方面表示,制药商可能准备在今年12月前提供第一批Paxlovid药片。基于此,分析公司Airfinity估计,更大的数量可能要到2023年5月才能进入市场。
此外,利托那韦口服片是辉瑞新冠口服药PAXLOVID(300毫克奈玛特韦片+100毫克利托那韦片组合包装)的组成之一。据国家药品监督管理局(NMPA)信息,截至目前,国内共有四家企业获批生产利托那韦,分别为歌礼药业、迪赛诺化学、万全万特制药、东阳光药业。据歌礼制药-B(01672)公布,已将利托那韦口服片年产能进一步扩大至约5.3亿片,以满足国内和全球日益增长的潜在需求。此外,歌礼已通过欧洲代理商向12个欧洲国家递交了利托那韦(100毫克薄膜衣片)上市许可申请。此外,精华制药、海特生物均具有成熟的利托那韦片关键中间体生产技术。

如此,在供应规模提升拉动供应链需求扩张之下,后续整个中国原料药市场又会发生怎样的调整,值得关注。
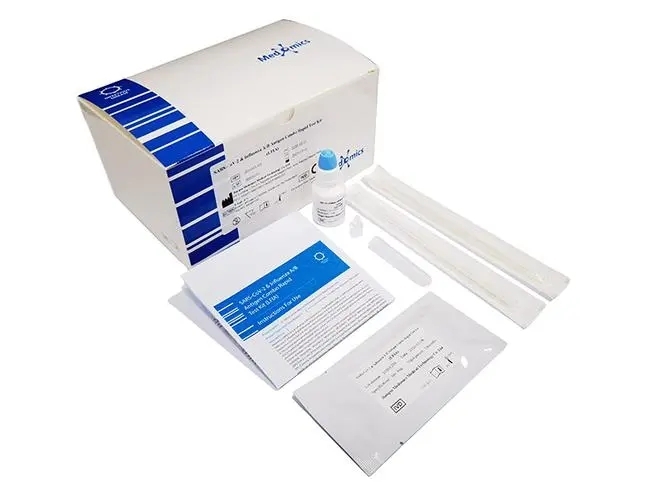
试剂盒产能及需求有多大?
3月11日,国务院应对新型冠状病毒肺炎疫情联防联控机制综合组印发了《新冠病毒抗原检测应用方案(试行)》(下称《方案》),决定在核酸检测基础上增加抗原检测作为补充。
截至3月18日,国家药监局已批准新型冠状病毒核酸检测试剂盒38个、抗体检测试剂盒36个、抗原检测试剂盒17个,助力疫情防控!
从东方基因(浙江东方基因生物制品股份有限公司研发生产的新型冠状病毒抗原检测试剂盒通过国家药监局注册审批)的数据来看“每天能生产1000万份以上,产量还可以扩大”。浙江省药品监督管理局药品安全总监董耿介绍说。
国家药监局新型冠状病毒检测试剂注册91家,规模不等。
新冠抗原检测,在进行大规模、快速筛查检测时,具有较高的社会价值,据有关分析预计,理性角度结合三类应用场景,基层医疗卫生机构诊疗检测需求市场规模约55亿,隔离观察人员检测需求约25亿,社区居民自检需求约249亿,整体合计超300亿。

根据海关总署数据,2021年中国累计向海外出口668.93亿的新冠检测试剂盒,2021年12月单月出口超100亿,其中迈克生物、华大基因、迪安诊断、明德生物、九安医疗、东方生物、热景生物等公司均已获得海外新冠抗原试剂上市资质。
包装商机
NC膜、PVC胶板、纸盒、塑料包材、自动包装机、喷码机的需求或将有数十亿的市场增量。